14.08.2025
Komplexbildung zwischen ACID RED 266 und CTAB in wässriger Lösung Teil 3: Spektroskopische Analyse der AR-CTAB-Aggregate
Teil 1 der Artikelserie beschreibt die Aggregation von ACID RED 266 (AR) in Wasser mittels UV/VIS-Spektroskopie und statischer Lichtstreuung. Teil 2 untersucht die Komplexbildung des anionischen Azofarbstoffs AR mit dem kationischen Tensid CTAB in Wasser mittels UV/VIS-Spektroskopie sowie dynamischer und elektrophoretischer Lichtstreuung.
Wie ausführlich in [7] beschrieben, lassen sich aus einem rechnerisch ermitteltem "Dimerspektrum" von AR in Wasser unter Anwendung der Excitonentheorie [22-25] wichtige geometrische Parameter wie der Twistwinkel β und der Interplanarabstand Ri der miteinander wechselwirkenden Moleküle gewinnen (Abbildung 16).
Den Formalismus dafür lieferten Mc Rae et al. sowie Kasha et al. indem sie die exzitonischen Wechselwirkungen in kristallinen Festkörpern auf Farbstoffaggregate übertragen haben.
Vereinfacht ausgedrückt stellen Excitonen einen elektronischen Anregungszustand dar, der sich über ein mehr oder weniger geordnetes System, wie in einem hoch geordneten kristallinen Festköper, wie z.B. im Fall von Pyren, oder auch über eine gestapelte Anordnung geringerer Ordnung als kristallin von z.B. Licht-absorbierenden Chlorophylleinheiten in photosynthetisch aktiven Systemen räumlich erstreckt. Hierbei werden vereinfachend die wechselwirkenden Einheiten als Punktdipole angenähert. Auf diese Weise können dann z.B. Wellenlängenverschiebungen in Abhängigkeit des Twistwinkels β erklärt werden, welche häufig bei einer Aggregation Licht-absorbierender Moleküle experimentell beobachtet werden.
Für 72 µM AR in Gegenwart von 10 mM CTAB zeigt das gemessene UV/VIS-Spektrum eine große Ähnlichkeit zu dem in [7] beschriebenen Dimerspektrum ohne Tensid. Aus diesem Grund soll es auf ähnliche Weise analysiert werden - wohlwissend, dass das untersuchte Objekt größer als ein Dimer ist. Es wurde eine Spektrenzerlegung wie in [7] vorgenommen, um zunächst die H- und J-Banden zu isolieren, wie in Abbildung 17 dargestellt.
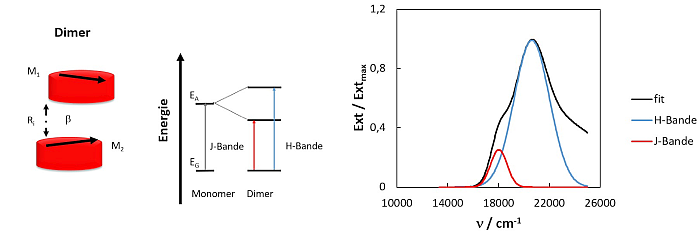
Abb.16 (links): Schematische Darstellung eines Stapel-Dimers mit Energiediagramm. EG beschreibt das Niveau des Grundzustands und
EA den des angeregten Zustands des Monomers. Die H- und J-Übergänge im Dimer sind ebenfalls dargestellt.
Abb.17 (rechts): Normiertes Spektrum von 72 µM AR in Gegenwart von 1 mM CTAB mit H- und J-Bande nach Spektrenzerlegung.
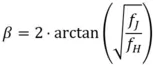
(Gln. 4)
β: Twistwinkel in °
fJ: Oszillatorstärke der J-Bande (dimensionslos)
fH: Oszillatorstärke der H-Bande (dimensionslos)
![]()
(Gln. 5)
f: Oszillatorstärke (dimensionslos)
ε: Extinktionskoeffizient als Funktion der Wellenzahl in L mol-1 cm-1
ν: Wellenzahl in cm-1
Über den Twistwinkel β lässt sich zudem der Interplanarabstand Ri berechnen:
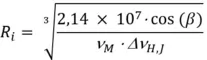
(Gln. 6)
Ri: Interplanarabstand in nm
νM: Wellenzahl des Monomerspektrums im Absorptionsmaximum (νM= 19.880 cm-1)
ΔνH,J: Dimerenaufspaltung, Differenz zwischen den Wellenzahlen der H- und der J-Bande (ΔνH,J = 2.600 cm-1)
Der Twistwinkel wurde mit β = 43° und der Interplanarabstand mit Ri = 0,67 nm bestimmt. Für AR in Wasser ohne NaCl bzw. ohne CTAB wurden β = 50° und Ri = 0,69 nm ermittelt [7].
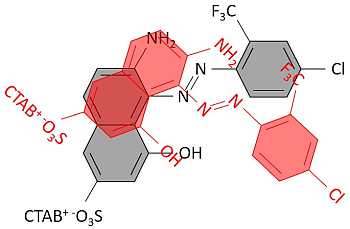
- Abb.18: Schematische Darstellung eines AR-CTAB-Komplexes
mit einem Twistwinkel von 43°.
Der Twistwinkel β = 43° liefert einen Modell-Vorschlag für eine mittlere Anordnung der miteinander wechselwirkenden Moleküle in einem AR-CTAB-Komplex in Lösung mit einer ungefähren Zusammensetzung von AR:CTAB = 1:1, die zweifarbig in Abbildung 18 dargestellt sind. Diese Anordnung unterscheidet sich nur geringfügig von derjenigen, die für ein "AR-Dimer" in Wasser bestimmt wurde [7].
Einfluss der Umgebung bei hoher CTAB-Konzentration
Wie bereits in Abbildung 10 erkennbar, bewegt sich λmax oberhalb der cmc von CTAB auf einen Plateauwert zu. Bereits ab der ca. 10-fachen cmc war mittels DLS keine Streuintensität mehr messbar, sodass kein hydrodynamischer Radius sowohl für die AR-Aggregate als auch für die CTAB-Mizellen ermittelt werden konnte. Die Form des Spektrums erinnert an das von AR in Ethylenglykol [27], in dem offensichtlich keine Farbstoffaggregate anwesend sind.
Unter der Annahme, dass bei etwa 10-100-facher cmc die Farbstoffaggregate weitgehend abgebaut wurden und wahrscheinlich molekulardispers gelöst im Inneren der CTAB-Mizellen vorliegen, muss dies Auswirkungen auf die Mikroumgebung der Farbstoffmoleküle und somit auf die Form des Absorptionsspektrums und die Lage des Absorptionsmaximums haben. Hierbei stellen die Alkylketten der CTAB-Moleküle die Umgebung eines organischen Lösemittels für ein Farbstoffmolekül dar, so dass von einer niedrigeren Dielektrizitätskonstante (DK) als der von Wasser (80) ausgegangen werden kann [28]. Hunter hat die DK von CTAB-Alkylresten mit ca. 30 abgeschätzt [29]. Die DK von Ethylenglykol, wie in [27] verwendet, liegt bei 48 [28], die von Methanol bei 33 [28].
Wenn die Farbstoffmoleküle bei hohen CTAB-Konzentrationen tatsächlich weitgehend molekulardispers gelöst in den Mizellen vorliegen, dann sollte sich das entsprechende UV/VIS-Spektrum in analoger Weise über eine Summe symmetrischer Gauß-Banden mit gleicher Bandenseparation, wie für Ethylenglykol in [27] beschrieben, analysieren lassen. Die Anwesenheit von Farbstoffaggregaten sollte sich durch Bandenverschiebungen, wie zuvor beschrieben, entsprechend bemerkbar machen.
Folgendes Modell wurde aufgestellt:
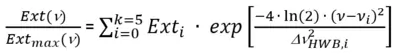
(Gln. 7)
Ext: Extinktion
Extmax: maximale Extinktion
Exti: Extinktion der Bande i
ν: Wellenzahl in cm-1
νi: Wellenzahl der Bande i
ΔνHWB,i: Halbwertsbreite der Bande i in cm-1
i: Laufzahl 1, 2, 3, ...
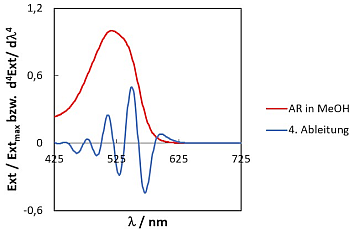
- Abb.19: Normiertes Spektrum von AR in MeOH (rot) mit
4. Ableitung (blau). Die Maxima der 4. Ableitung liegen
im Mittel um 1350 cm-1 von einander separiert vor.
(Gln. 8)
νlangwellig = 17.881 cm-1
i: Laufzahl 1, 2, 3, ...
Δννib = 1350 cm-1
(Gln. 9)
FQS: Fehlerquadratsumme
Y(ν)berechnet,i = Ext(ν)berechnet,i / Extmax: berechnete normierte Extinktion für den Datenpunkt i
Y(ν)gemessen,i = Ext(ν)gemessen,i / Extmax: gemessene normierte Extinktion für den Datenpunkt i
![]()
(Gln. 10)
Χ2: Χ2-Wert
n: Anzahl der Datenpunkte
p: Anzahl der fit-Parameter
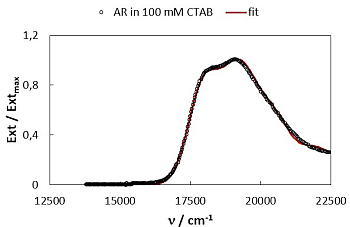
- Abb.20: Normiertes Absorptionsspektrum von 72 µM AR
in 100 mM CTAB im Vergleich zum berechneten.
Sie liefert somit ein starkes Argument dafür, dass die Farbstoffmoleküle bei der ca. 100-fachen cmc von CTAB sehr wahrscheinlich de-aggregiert im Inneren der Mizellen vorliegen. Für AR in MeOH wurde ein ähnlich niedriger Χ-Wert von 1,3 x 10-4 gefunden [27].
Abbildung 20 zeigt die gute Übereinstimmung zwischen dem gemessenen und dem nach den Gleichungen 7 bis 9 berechneten Spektrum.
Fazit - Modellvorschlag
Für die in dieser Arbeit beschriebenen Effekte soll ein Modell vorgeschlagen werden, dass sich im Wesentlichen auf drei Situationen in stark vereinfachter Weise konzentriert:
I. prämizellarer Bereich: < 5 x 10-5 M CTAB
II. Bereich der Komplexbildung: 6 x 10-5 M bis 8 x 10-4 M CTAB
III. postmizellarer Bereich: > 9 x 10-4 M CTAB
Im prämizellaren Bereich, also deutlich unterhalb der cmc von CTAB, liegen Farbstoffaggregate und CTAB-Moleküle vor, wobei die UV/VIS-Spektren kaum Veränderungen in der Höhe sowie in der Lage ihres Absorptionsmaximums zeigen. Die Zählraten der DLS sind zu gering, um bei der gegebenen Laserleistung der Primärlichtquelle messbare Teilchendurchmesser liefern zu können.
Der Bereich der Komplexbildung steckt den Bereich ab, in dem drastische hypsochrome sowie hypochrome Verschiebungen der UV/VIS-Spektren stattfinden. Ebenso werden hydrodynamische Radien messbar. Bei der cmc von CTAB liegen die elektrophoretischen Beweglichkeiten bei etwa Null, die hydrodynamischen Radien werden maximal und zeitabhängig. Es kommt sehr wahrscheinlich zu einer Assoziation von Farbstoffaggregaten über adsorbierte CTAB-Moleküle oder Aggregate. Die Farbstoffaggregate selbst können durch partielles Auflösen durch den Einfluss der Tensidmoleküle auch kleiner werden, wenngleich ein Zusammenschluss von mehreren über CTAB-Moleküle zusammengelagerten Farbstoffaggregaten recht groß werden kann mit RH = ca. 300 nm und mehr.
Für eine CTAB-Konzentration von 1 x 10-4 M konnte ein Modellvorschlag für einen AR-CTAB-Komplex in Lösung präsentiert werden, der sich nur wenig von dem in [7] in Abwesenheit von CTAB bestimmten "Dimer" unterscheidet (Twistwinkel β = 43°).
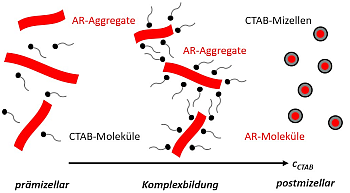
- Abb. 21: Vereinfachte schematische Darstellung der Aggregations-
und De-Aggregationsprozesse von AR in
Abhängigkeit der CTAB-Konzentration.
Die gemessenen UV/VIS-Spektren werden von hyperchromen und bathochromen Effekten begleitet, was in Einklang steht mit einem Abbau der Farbstoff-Aggregate sowie einem Wechsel der Mikroumgebung für AR-Moleküle von polar (Wasser) nach unpolar (Alkylketten der CTAB-Mizellen, die wie ein organisches Lösemittel aufgefasst werden können).
Eine Anpassung des in Gegenwart von 100 mM CTAB gemessenen UV/VIS-Spektrums von AR auf der Basis eines Modells, das bereits für den gleichen Farbstoff in Ethylenglykol angewendet wurde [27], macht das beschriebene Szenario plausibel.
Die in Abbildung 21 skizzierten Kugelmizellen wurden willkürlich gewählt. Es ist ebenso möglich, dass ellipsoide oder evtl. sogar zylinderförmige Mizellen in Gegenwart der Farbstoffmoleküle vorliegen. Ihr Radius kann jedoch nicht sehr groß sein, da keine ausreichende Streuintensität detektiert werden konnte. Eine Bildung von Riesenmizellen, induziert durch die Farbstoffmoleküle, wäre ebenfalls denkbar. Allerdings wurde kein zusätzlicher Elektrolyt, wie z.B. NaCl hinzugefügt, der ein solches Wachstum begünstigen würde, wie z.B. in [30] dargelegt.
Literatur
- H.-D. Dörfler, Grenzflächen- und Kolloidchemie, VCH-Verlag Weinheim 1994, 206
- N. Khan, B. Brettmann, Polymers 2019, 11, 51
- D. Voet, J.G. Voet, Biochemistry, John Wiley & Sons, Inc. 1995, 862
- H.-D. Dörfler, Grenzflächen- und Kolloidchemie, VCH-Verlag Weinheim 1994, 225
- R.D. Wesley, T. Cosgrove, L. Thompson, S.P. Armes, F.L. Baines, Langmuir 2002, 18, 5704
- A.R. Monahan, D.F. Blossey, J. Phys. Chem. 1970, 74, 4014
- B. Neumann, K. Huber, P. Pollmann, Phys. Chem. Chem. Phys. 2000, 2, 3687
- R.L. Reeves, M.S. Maggio, S.A. Harkaway, J. Phys. Chem. 1979, 83, 2359
- K. Hamada, S. Take, T. Iijima, S. Amiya, J. Chem. Soc., Faraday Trans. 1, 1986, 82, 3141
- H.-D. Dörfler, Grenzflächen- und Kolloidchemie, VCH-Verlag Weinheim 1994, 412
- W. Burchard, Static and Dynamic Light Scattering from Branched Polymers and Biopolymers, Springer Verlag 1983, 48, 58
- P. Denkinger, W. Burchard, J. Polym. Sci, Polym. Phys. 1991, 29, 589
- R. Koyama, J. Phys. Soc. Jpn. 1973, 34, 1029
- J. Israelachvili, Intermolecular & Surface Forces, Academic Press 1991, New York, 355
- C. Bellmann, A. Caspari, C. Moitzi, F. Babick, Dynamische und elektrophoretische Lichtstreuung 2020, 59, Anton Paar GmbH
- C. Bellmann, A. Caspari, C. Moitzi, F. Babick, Dynamische und elektrophoretische Lichtstreuung 2020, 61, Anton Paar GmbH
- C. Bellmann, A. Caspari, C. Moitzi, F. Babick, Dynamische und elektrophoretische Lichtstreuung 2020, 95, Anton Paar GmbH
- H. Stroppe, Physik, Fachbuchverlag Leipzig 2005, 310
- J. Israelachvili Intermolecular & Surface Forces, Academic Press 1991, New York, 355
- C. Bellmann, A. Caspari, C. Moitzi, F. Babick, Dynamische und elektrophoretische Lichtstreuung 2020, 33, Anton Paar GmbH
- J. Israelachvili Intermolecular & Surface Forces, Academic Press 1991, New York, 246
- M. Kasha, H.R. Rawls, M. Ashraf El-Bayoumi, Pure and Applied Chemistry 1965, 11, 371
- E.G. McRae, Aust. J. Chem. 1961, 14, 229
- E.G. McRae, Aust. J. Chem. 1961, 14, 344
- E.G. McRae, Aust. J. Chem. 1961, 14, 354
- G.J.T. Tiddy, D.L. Mateer, A.P.Omerod, W.J. Harrison, D.J. Edwards, Langmuir, 1995, 11, 390.
- B. Neumann, Dyes and Pigments, 2002, 52, 47
- J. Israelachvili Intermolecular & Surface Forces, Academic Press 1991, New York, 80
- R.J. Hunter, Foundations of Colloid Science, Oxford University Press 2001, 465
- C.N. Lam, C. Do, Y. Wang, G.-R. Huang, W.-R. Chen, Phys. Chem. Chem. Phys. 2019, 21, 18346
Danksagung
Teile dieser Arbeit entstanden im Zeitraum von 2000-2004 an den Universitäten Hull, UK und Bristol, UK. Der Autor bedankt sich bei Prof. P.D.I. Fletcher (Universität Hull), Prof. B. Vincent und Prof. J. Eastoe (beide Universität Bristol) für die Bereitstellung diverser Geräte. Der Farbstoff Acid Red 266 wurde von Prof. G.J.T. Tiddy (Universität Salford, UK) zur Verfügung gestellt. Leider sind Prof. Tiddy und Prof. Pollmann (Universität Paderborn) kürzlich verstorben. Beiden gemeinsam war eine direkte, humorvolle und sehr menschliche Art.
