18.03.2021
Entwicklung einer neuen Derivatisierungsreaktion von Perfluorcarbonsäuren mit N,N-Dimethylformamid-Dialkylacetalen
Dr. Kathrin Schuhen , Wasser 3.0
Dr. Monika Breithaupt, SAS Hagmann GmbH
N,N-Dimethylformamid-Dialkylacetale sind sehr leistungsfähige Derivatisierungsreagenzien. Das bekannteste Mitglied dieser Gruppe ist N,N-Dimethylformamid-Dimethylacetal oder kurz DMF-DMA. Wir haben versucht, diese Verbindung zu verwenden, um Perfluoroctansäure (PFOA) zu derivatisieren und einen Ester zu bilden. Unsere Untersuchungen zeigten jedoch, dass der Ester bei dieser Reaktion nur als Nebenprodukt entsteht.
Für die Strukturuntersuchung des unbekannten Hauptprodukts wurden verschiedene massenspektrometrische Techniken verwendet, z.B. Elektronenionisation (EI), Elektrospray-Ionisation (ESI) und direkte Analyse in Echtzeit (engl. direct analysis in real time DART). Wir fanden heraus, dass bei der Reaktion von PFOA mit DMF-DMA im organischen Lösungsmittel ein Salz gebildet wird.
Darüber hinaus reagiert das Salz unter CO2-Abspaltung im Injektionsblock eines Gaschromatographen (GC) weiter. Das Hauptprodukt der Derivatisierung, das im GC-MS-Chromatogramm gefunden wurde, war 1,1-Perfluoroctan-(N,N,N,N-Tetramethyl)-diamin. Die detaillierte Untersuchung der Reaktionsprodukte mittels Massenspektrometrie wurde in unserer früheren Veröffentlichung [1] beschrieben. In diesem Mini-Review werden die wichtigsten Ergebnisse dieser Forschung vorgestellt.
Einführung
Perfluorcarbonsäuren (PFCAs) sind anthropogene Chemikalien mit sehr nützlichen Eigenschaften und vielen industriellen Anwendungen. Allerdings haben diese Verbindungen auch bereits beschriebene negative Auswirkungen auf die menschliche Gesundheit. Mehrere Studien haben Neurotoxizität, Reproduktionstoxizität und Entwicklungstoxizität von PFCAs nachgewiesen [2]. Daher werden zuverlässige Analysemethoden benötigt, um die Konzentration von PFCAs in Lebensmitteln, Wasser, Umweltproben und Alltagsprodukten zu kontrollieren. Derzeit ist Flüssigchromatographie gekoppelt mit Massenspektrometrie (LC-MS/MS) die am häufigsten angewandte Technik zur Analyse von PFCAs. Auch mehrere gaschromatographische Methoden, wie z.B. Veresterung [3], Silylierung [4] und die Bildung von Aniliden [5], um die bekanntesten zu nennen, wurden veröffentlicht. Die wichtigsten Vorteile der GC-MS-Analyse sind: hohe Auflösung, eine umfangreiche Spektrenbibliothek, geringe Analysenkosten und relativ einfache Methodenentwicklung [6].
Warum DMF-DMA?
DMF-DMA ist ein bekanntes Alkylierungsmittel, das unter dem Namen Methyl-8® gelöst in Pyridin auf dem Markt erhältlich ist. Diese Verbindung hat sowohl eine elektrophile als auch eine nukleophile Komponente in ihrer Struktur und ist daher sehr reaktiv. Das Kohlenstoffatom ist an drei elektronenziehende Gruppen (zwei Methoxy- und eine Dimethylaminogruppe) gebunden, die die elektrophile Stelle bilden. Als nukleophile Komponente dient das einzelne Elektronenpaar des an zwei Methylgruppen und ein Kohlenstoffatom gebundenen Stickstoffatoms [7]. Um eine einfache Derivatisierungsmethode für PFCA in organischer Lösung zu entwickeln, untersuchten wir die Reaktionen von N,N-Dimethylformamid-Dialkylacetalen mit Perfluorcarbonsäuren.
Die Bildung von Methylestern der PFCA mit DMF-DMA und deren Analyse mittels GC-FID wurde bereits 1977 von Eliott beschrieben [8]. Er fand heraus, dass eine geringe Menge Wasser notwendig ist, um die Reaktion zu katalysieren. Das erste Ziel unserer Forschung war es, die von Eliott beschriebene Methode für die Verwendung von GC-MS-Systemen anzupassen. Da Wasser jedoch die Empfindlichkeit des Massenspektrometers verschlechtert, konnten die Reaktionsbedingungen nicht direkt übernommen werden.
Aus diesem Grund wurde die Reaktion in organischem Lösungsmittel ohne Zugabe von Wasser durchgeführt [9]. Im Laufe der Untersuchungen stellte sich heraus, dass bei dieser Reaktion zwar ein Ester gebildet wird, dieser aber nur als Nebenprodukt auftritt. Wir vermuten, dass das Wasser die Veresterungsreaktion fördert und die gleiche Reaktion ohne Wasser zur Bildung eines anderen Hauptprodukts führt. Die Struktur des Hauptprodukts und wie es gebildet wird, war zu Beginn der Forschung nicht bekannt. Deshalb wurde die Strukturaufklärung dieses Produkts zum primären Ziel unserer Arbeit.
Zusammensetzung der PFCA-Derivatisierungsprodukte
Für die Strukturuntersuchung des Hauptprodukts wurden verschiedene massenspektrometrische Analysen durchgeführt: Elektrospray-Ionisation (ESI), Direktanalyse in Echtzeit (DART), Flüssigkeitsinjektionsfeld-Desorption/ Ionisation (engl. liquid injection field desorption/ionization LIFDI) und (in Kombination mit GC) Elektronenstoß-Ionisation (EI) sowie positive chemische Ionisation (PCI). Für alle massenspektrometrischen Analysen wurde Perfluoroctansäure (PFOA) in Acetonitril oder MTBE gelöst und mit DMF-DMA oder DMF-DEA vermischt. In einer optimierten Reaktion erfolgte die Derivatisierung durch Zugabe von 50 µl einer 0,4 M DMF-DMA-Lösung zu 200 μl PFCA-Lösung. Die Probe konnte ohne weitere Bearbeitung direkt in das GC-System injiziert werden.
Im ersten Schritt wurden GC-MS-EI-Analysen von zwei Reaktionsgemischen durchgeführt: PFOA mit DMF-DMA und PFOA mit DMF-DEA. Es wurde beobachtet, dass in beiden Reaktionen das gleiche Hauptprodukt (Peak 1 in Abbildung 1) gebildet wird. Dies zeigt, dass das detektierte Hauptprodukt kein Ester sein kann, da DMF-DMA und DMF-DEA unterschiedliche Ester bilden. Als Nebenprodukt entstand ein Ethylester (Peak 2 in Abbildung 1). Die Retentionszeit des Methylesters ist zu kurz und kann auf dem Chromatogramm nicht erkannt werden. Dieses Ergebnis deutet darauf hin, dass die Methoxy- oder Ethoxygruppen aus den Derivatisierungsmitteln nicht an der Bildung des Hauptprodukts beteiligt sind.
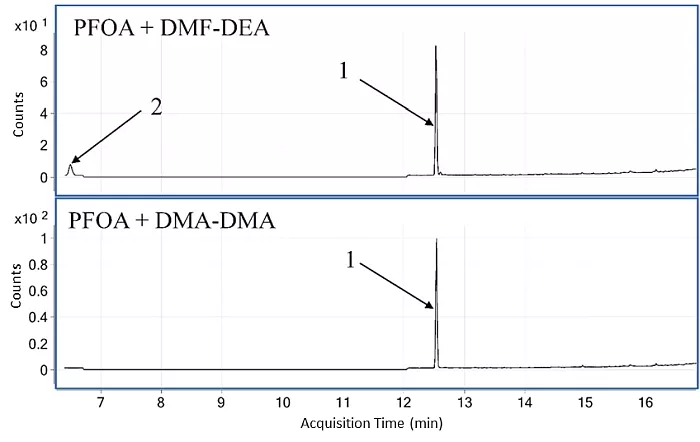
Abb.1: Chromatogramm zweier Proben nach der Derivatisierung von PFOA mit DMF-DEA (oben) und DMF-DMA (unten) [1]
Das EI-Spektrum des Hauptprodukts zeigte ein intensives Signal bei m/z 426, das intuitiv keinem logischen Produkt der Reaktion zugeordnet werden konnte (Abbildung 2).
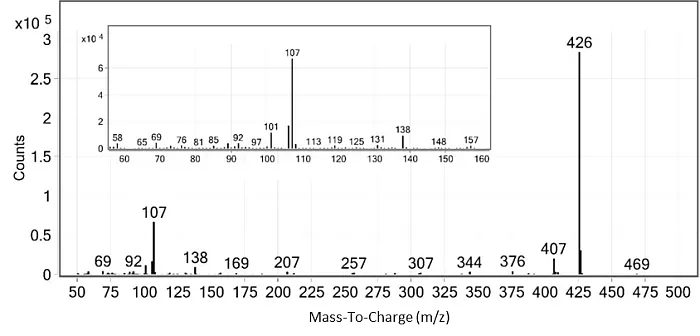
Abb.2: EI-Massenspektrum des unbekannten PFOA Derivatisierungsproduktes
in Korrelation mit Peak 1 des Chromatogramms aus Abbildung 1[1]
Als nächstes wurde eine GC-MS-PCI-Analyse durchgeführt. Neben dem Fragment-Ion bei m/z 426 konnten im PCI-Spektrum auch größere Fragment-Ionen bei m/z 442 und 451 beobachtet werden. Basierend auf diesen beiden Spektren wurde angenommen, dass die Masse der Verbindung 470 u beträgt. Ein kleines Signal bei m/z 469 im EI würde demnach einem Fragment [M-H]+ entsprechen. Das Fragment-Ion bei m/z 451 im PCI-Spektrum könnte dann vom Verlust von 19 u, also F-, stammen.
Im nachfolgenden Experiment wurde das unbekannte Produkt der Reaktion von PFOA mit DMF-DMA durch eine ESI und DART im positiven und negativen Ionenmodus analysiert. Das positive ESI-Spektrum ergab nur ein Signal bei m/z 615.1812, das nicht mit dem EI-Ergebnis in Zusammenhang gebracht werden konnte. Ähnlich wie bei der ESI ergab auch die positive DART-Analyse nur ein Ion bei m/z 615.1801. Das negative ESI-Spektrum zeigte ebenfalls ein Signal bei sehr hohem m/z: 927.0404. Die ESI- und DART-Ergebnisse führten zu der Vermutung, dass mehrere Cluster-Ionen in der Probe gefunden wurden. Da die Masse eines PFOA-Anions 413 u beträgt, könnte das Cluster-Ion mit m/z 927 aus zwei PFOA-Anionen und einem kleinen Kation mit der nominellen Masse 101 u bestehen. Diesem Gedankengang folgend, müsste ein Kation bei m/z 615 aus einem PFOA-Anion (413 u) und zwei massearmen Kationen (je 101 u) bestehen. Auf diese Weise wurde dem Kation des Cluster-Ions die Strukturformel [C5H13N2]+, ein Iminiumkation, zugeordnet. Damit konnte gezeigt werden, dass es sich bei dem unbekannten Hauptprodukt um ein Salz handeln muss.
Um dies zu beweisen, sollte ein Kation bei m/z 101 in der Probe nachgewiesen werden. Daher wurde als nächstes eine TOF-MS-Analyse mit Flüssigkeitsinjektionsfeld-Desorption/Ionisation (LIFDI) durchgeführt. Diese Messung ergab ein LIFDI-Spektrum mit einem Basispeak bei m/z 101,12, der dem Iminiumkation [C5H13N2]+ zugeordnet werden konnte.
Das Derivatisierungsmittel (DMF-DMA) durchläuft in Gegenwart von Perfluorcarbonsäure eindeutig eine Umlagerung und bildet ein sehr stabiles Kation, das bei m/z 101 nachgewiesen werden kann. In Lösung bildet sich ein N,N,N',N'-Tetramethylformamidinium-Salz von PFOA (Abbildung 3).
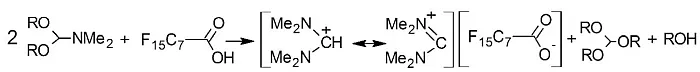
Abb.3: Bildung des Salzes der PFOA während der Umsetzung mit DMF-DMA [1].
Mit diesen Erkenntnissen konnten die GC-MS-EI-Daten überarbeitet werden, um zusätzliche Informationen zu erhalten. Da ein aus PFOA und DMF-DMA gebildetes Salz nicht mittels GC-MS nachgewiesen werden kann, musste eine weitere Reaktion innerhalb des Injektionsblocks des GCs stattgefunden haben. Eine Zersetzung des Salzes konnte ausgeschlossen werden, da diese Reaktion PFOA freisetzen würde, das als breiter Peak zu finden wäre. Da das Phänomen des CO2-Verlustes aus einer Halo-Essigsäure im GC-Injektor bereits in der Literatur beschrieben wurde [10, 11], lag die Möglichkeit einer Decarboxylierung als Reaktion dieses Salzes im Injektor nahe. Abbildung 4 zeigt die Decarboxylierung im Injektor und das Hauptprodukt der Reaktion.
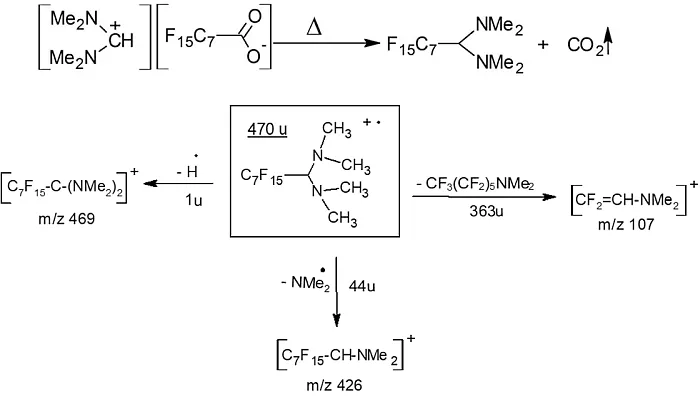
Abb.4: Die Reaktion des PFOA-Salzes in der Injektionskammer [1] und die wichtigsten Fragment-Ionen des Hauptprodukts (1-Perfluoroctan-(N,N,N-tetramethyl)-diamin).
Forschung versus praktische Anwendung
Nachdem der Reaktionsmechanismus und das Produkt identifiziert waren, folgte eine Optimierung der Reaktion für die PFCA-Analyse von Extrakten fester Proben. Eine Kurzschrift über diese Forschung wurde bereits veröffentlicht [12]. Es wurde der Einfluss von Lösungsmittel, Reaktionszeit und Temperatur getestet. Während Alkohole und Pyridin die Veresterungsreaktion begünstigen, sind unpolare Lösungsmittel, wie Hexan und MTBE, gut für die Aminbildung geeignet. Darüber hinaus wurde nach umfangreichen Untersuchungen zu Matrixeffekten auf die Reaktion festgestellt, dass für die Quantifizierung von PFCA in realen Proben die Standardadditionsmethode am besten geeignet ist. Die Methode konnte erfolgreich für drei Arten von Proben angewendet werden: Zahnseide, Textilien und Klärschlamm.
Ausblick
Diese Methode hat das Potenzial, in vielen Laboren für die PFCA-Analyse eingesetzt zu werden, da die Reaktion sehr schnell und einfach und die Probenvorbereitung in wenigen Schritten erledigt ist. Außerdem ist für die Durchführung dieser Reaktion keine spezielle Laborausrüstung erforderlich. GC-MSD ist eine der einfachsten Kopplungen von gaschromatographischer Trennung und massenspektrometrischer Detektion. Dies qualifiziert die entwickelte Methode dazu, in vielen analytischen Laboratorien zu einer analytischen Standardmethode für PFCA zu werden, da GC-MSD-Systeme kostengünstiger und einfacher zu bedienen sind als LC-MS/MS-Systeme.
Danksagung
Die Autoren bedanken sich für die technische und wissenschaftliche Unterstützung durch die SAS Hagmann GmbH (Horb, Deutschland).
Literatur
- Strozynska M, Gross JH, Schuhen K. Structural investigation of perfluorocarboxylic acid derivatives formed in the reaction with N,N-dimethylformamide dialkylacetals. Eur J Mass Spec 2019;30.
- Stahl T, Mattern D, Brunn H. Toxicology of perfluorinated compounds. Environ Sci Eur 2011;23(38):1-52.
- Jurado-Sánchez B, Ballesteros E, Gallego M. Semiautomated solid-phase extraction followed by derivatisation and gas chromatography-mass spectrometry for determination of perfluoroalkyl acids in water. J Chromatogr A 2013;1318:65-71.
- Lv G, Wang L, Liu S, et al. Determination of perfluorinated compounds in packaging materials and textiles using pressurized liquid extraction with gas chromatography-mass spectrometry. Anal Sci 2009;25(3):425-29.
- Scott BF, Moody CA, Spencer C, et al. Analysis for perfluorocarboxylic acids/anions in surface waters and precipitation using GCMS and analysis of PFOA from large-volume samples. Environ Sci Technol 2006;40(20):6405-10.
- Strozynska M, Schuhen K. Dispersive solid-phase extraction followed by triethylsilyl derivatization and gas chromatography mass spectrometry for perfluorocarboxylic acids determination in water samples. J of Chromatogr A 2019;1597:1-8.
- Abu-Shanab FA, Sherif SM, Mousa SAS. Dimethylformamide dimethyl acetal as a building block in heterocyclic synthesis. J Heterocyclic Chem 2009;46(5):801-27.
- Elliott DE. Anomalous Response off the Flame lonization Detector to Perfluorinated Carboxylic Acids. J Chromatogr Sci 1977;15(10):475-77.
- Monika Strozynska. Entwicklung neuer Derivatisierungsmethoden für die GC-MS Analyse von Perfluorcarbonsäuren in variablen Probenmatrices. PhD Thesis. University of Koblenz-Landau, Germany; 2020.
- Drechsel D, Dettmer K, Engewald W, et al. GC Analysis of trichloroacetic acid in water samples by large-volume injection and thermal decarboxylation in a programmed-temperature vaporizer. Chromatographia 2001;54(3-4):151-54.
- Xie Y. Analyzing haloacetic acids using gas chromatography/mass Spectrometry. Water Res 2001;35(6):1599-602.
- Strozynska M, Schuhen K. Derivatization of perfluorocarboxylic acids with N,N-dimethylformamide dimethylacetal prior to GC-MS analysis. Chromatographia 2020;83(3):477-82.
