10.02.2022
Die relative Kalibrierung in der Gelpermationschromatographie
Dr. Gerhard Heinzmann , Alina Heinzmann, Sophia Heinzmann
Warum es wissenschaftlich korrekt sein kann, Äpfel mit Birnen zu vergleichen
Es gibt im Bereich der Polymeranalytik viele etablierte Methoden, mit denen man das Molekulargewicht und die Molekulargewichtsverteilung einer makromolekularen Probe bestimmen kann. Hier sind zum Beispiel die Methode der Endgruppenanalyse und der Membranosmometrie zu nennen, weiterhin die Lichtstreuung, die Viskosimetrie und auch die Ultrazentrifugation.
Jede dieser Methoden bestimmt das mittlere Molekulargewicht einer Probe, aber nicht immer denselben Mittelwert. Aus der statischen Lichtstreuung resultiert z. B. das nach dem Gewicht gemittelte Molekulargewicht Mw einer makromolekularen Probe, während die Endgruppenanalyse das Zahlenmittel Mn bestimmt. Aus der Ultrazentrifugation wiederum resultiert das Zentrifugenmittel Mz.
Die verschiedenen Methoden sind daher auch unterschiedlich sensitiv auf bestimmte Probenanteile. So reagieren die Endgruppenanalyse und die Membranosmometrie eher auf niedermolekulare Probenanteile, während die Viskosimetrie und auch die Ultrazentrifugation mehr auf die hochmolekularen Probenanteile ansprechen.
Eine besondere Methode in der Polymeranalytik stellt die Gelpermeationschromatographie (GPC), auch Größenausschlusschromatographie genannt (SEC = Size Exclusion Chromatography), dar [1]. Mit Ihrer Hilfe können alle Molekulargewichtsmittelwerte, und auch die Verteilung der Molekulargewichte in einer Makromolekularen Probe, bestimmt werden.
In Ihrer einfachsten Form, der so genannten konventionellen oder relativen Kalibrierung, ist ein GPC/SEC-System nur mit einem Konzentrationsdetektor ausgestattet. Es wird eine Kalibrierkurve mit Polymerstandards, mit bekanntem Molekulargewicht, über das Elutionsvolumen erstellt. Über den Vergleich mit dieser Kalibrierkurve werden nun die Molekulargewichte von unterschiedlichen Proben bestimmt.
Obwohl die Resultate eigentlich als falsch bezeichnet werden müssten, sobald die chemische und molekulare Struktur der Probe nicht mit der chemischen und molekularen Struktur der verwendeten Kalibrierstandards übereinstimmt, sind die Resultate dieser Technik wissenschaftlich anerkannt. Im Folgenden soll aufgezeigt werden, warum dies der Fall ist.
Erstellung einer relativen Kalibrierkurve in der GPC/SEC
Die Erstellung einer relativen Kalibrierkurve mit einem GPC/SEC-System ist sehr einfach. Das GPC/SEC-System verfügt meist nur über einen Konzentrationsdetektor. Im Vergleich zu HPLC-Systemen, wo überwiegend UV- und Diodenarraydetektoren eingesetzt werden, hat sich in der GPC/SEC der Brechungsindexdetektor (RI = Refractive Index Detector) durchgesetzt, aus dem einfachen Grund, dass viele handelsübliche Polymere keine chromophoren Gruppen enthalten, und somit einer UV-Detektion nicht zugänglich sind. Der Anwender kann am Markt von verschiedenen Herstellern eine Reihe von eng verteilten, sehr gut charakterisierten Polymerstandards kaufen.
Für den organischen Bereich haben sich Polystyrole und PMMA etabliert, im wässrigen Bereich werden überwiegend Pullulane und Polyethylenoxide (PEO) eingesetzt. Alle diese Polymerstandards weisen eine lineare Struktur ohne Verzweigungen im Molekül auf. Der Anwender muss diese Standards nun vermessen, wobei in der resultierenden Kalibrierkurve in der Regel das Peak-Molekulargewicht Mp des jeweiligen Polymerstandards gegen dessen Elutionsvolumen aufgetragen wird. Eine entsprechende Kalibrierkurve ist in Abbildung 1 aufgetragen.
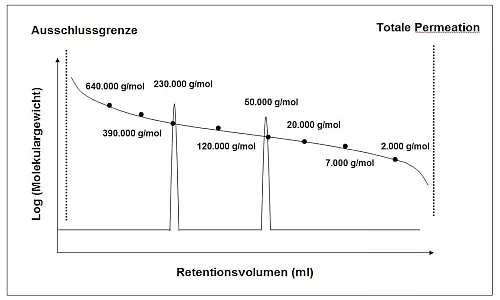
Abb.1: Relative Kalibrierkurve mit eng verteilten Polymerstandards.
Angegeben sind die Werte für das Peak-Molekulargewicht (Mp) der Polymerstandards.
Da eine einzige Mixed-Bed Trennsäule aufgrund der breiten Porengrößenverteilung aber keine sehr effektive Trennleistung erzielt, werden oft zwei oder drei Mixed-Bed Trennsäulen mit identischer Porengrößenverteilung hintereinander verwendet. Bei geringen Elutionsvolumina steigt die Kalibrierkurve ins Unendliche an, weil hier die so genannte Ausschlussgrenze erreicht ist. Polymermoleküle, die eine bestimmte Größe überschreiten, werden von den Trennsäulen nicht mehr aufgetrennt.
Der identische Fall tritt bei sehr großen Elutionsvolumina auf. Hier führt das Phänomen der Totalen Permeation dazu, dass Polymermoleküle, die eine bestimmte Größe unterschreiten, ebenfalls von den Trennsäulen nicht mehr weiter aufgetrennt werden können.
Messung einer unbekannten Probe
Hat der Anwender nun erfolgreich eine Kalibrierkurve mit linearen, eng verteilten Polymerstandards erstellt, dann kann er mit der Messung von unbekannten Proben beginnen. Ein großer Vorteil der Technik der relativen Kalibrierung liegt darin begründet, dass der Anwender so gut wie nichts über seine Probe wissen muss.
Eine exakte Konzentration der Probe ist für die Bestimmung des Molekulargewichtes nicht relevant. Die Probe muss sich nur im gewählten Lösungs- und Laufmittel lösen, und die Konzentration muss hoch genug sein, damit bei der Messung der Probe ein auswertbarer Probenpeak entsteht, sie darf aber nicht zu hoch sein, so dass das Signal des Konzentrationsdetektors nicht in die Sättigung läuft.
Von dem Peak der durch die Probe erzeugt wird, kann nun das Elutionsvolumen bzw. die Retentionszeit an der Peakspitze bestimmt werden. Dieses Elutionsvolumen vergleicht der Anwender mit der zuvor erstellten Kalibrierkurve wie in Abbildung 2 dargestellt.
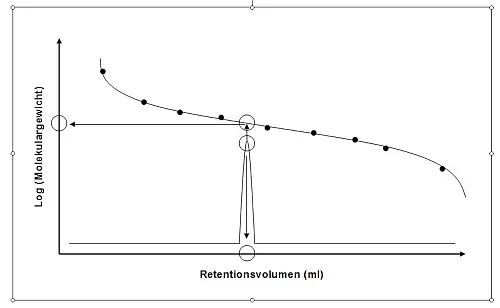
Abb.2: Bestimmung des Peak-Molekulargewichtes einer unbekannten Polymerprobe.
Ist die Probe allerdings keine lineare Polystyrolprobe, sondern ein anderes Polymer, dann spricht man von so genannten Polystyroläquivalenten. Das Peak-Molekulargewicht der unbekannten Probe ist dann äquivalent zu dem aus der mit linearen Polystyrolstandards erstellten Kalibrierkurve resultierenden Molekulargewicht. Diese Aussage ist wissenschaftlich absolut korrekt und reproduzierbar, völlig unabhängig davon, um welchen Polymertyp es sich bei der unbekannten Probe handelt, und welche molekulare Struktur die Probe aufweist.
Verschiedene Polymertypen, wie z. B. Polycarbonat, weisen eine deutlich kettensteifere Molekülstruktur auf im Vergleich zu Polystyrol. Da die GPC/SEC-Trennsäulen aber nur nach dem hydrodynamischen Radius der Polymermoleküle trennen, eluieren Polycarbonatmoleküle mit gleichem Molekulargewicht deutlich früher als Polystyrolmoleküle, wodurch sie ein zu hohes, relatives Molekulargewicht vortäuschen, wenn sie mit der Technik der relativen Kalibrierung gemessen werden.
Verzweigte Polymere hingegen haben in der Regel bei gleichem Molekulargewicht einen sehr viel geringeren hydrodynamischen Radius als Polystyrolmoleküle, da die Verzweigungen zu einer höheren Dichte des Polymerknäuels führen. Sie würden bei gleichem Molekulargewicht daher deutlich später eluieren als lineare Polystyrolmoleküle und somit ein deutlich geringeres, relatives Molekulargewicht vortäuschen.
Obwohl also die Ergebnisse, die man mit der Methode der relativen Kalibrierung erzielt, nicht der Wahrheit entsprechen, also nicht das wirklich vorhandene Molekulargewicht einer Probe abbilden, sind diese Ergebnisse wissenschaftlich dennoch anerkannt. Wichtig ist nur der Punkt, dass sie reproduzierbar sind.
Wenn ein Anwender irgendwo auf der Welt dieselben Messungen durchführt, also dieselbe Probe gegen eine Reihe von linearen Polystyrolstandards misst, dann wird er zum selben relativen Ergebnis kommen, auch wenn dies nicht dem realen Wert entspricht. Allein diese Reproduzierbarkeit genügt dem wissenschaftlichen Anspruch, es wird kein Wert auf ein korrektes, real vorliegendes Ergebnis gelegt.
Bestimmung von absoluten Polydispersitäten und absoluten Mn-Werten
Eine weitere Stärke der Methode der relativen Kalibrierung in der GPC/SEC ist darin begründet, dass man mit dieser Technik nicht nur das Molekulargewicht der Probe an der Peakspitze messen kann, sondern an jedem Punkt des Peaks. Summiert man alle diese einzelnen Molekulargewichte auf, dann kann man Mittelwerte bilden. Der einfachste Mittelwert ist das nach der Anzahl der Moleküle gemittelte Molekulargewicht Mn (Number Average Molecular Weight):
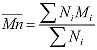
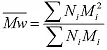
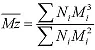
Neben den drei Molekulargewichtsmittelwerten Mn, Mw und Mz, gibt es noch das so genannte Peak-Molekulargewicht Mp, das den Wert für das Molekulargewicht einer makromolekularen probe an der Peakspitze der differentiellen Molekulargewichtsverteilung beschreibt (Abbildung 3).
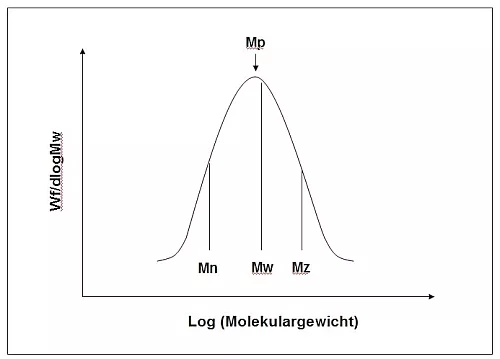
Abb.3: Differentielle Molekulargewichtsverteilung einer breit verteilten,makromolekularen Probe mit mittleren Molekulargewichten
Interessant ist die Tatsache, dass, selbst wenn die Struktur der Probe von der Struktur der für die Erstellung der relativen Kalibrierkurve verwendeten Polymerstandards abweicht und daher die ermittelten Molekulargewichte nicht absolut sind, man dennoch einen absoluten Wert für die Polydispersität erhält. Dies eröffnet auch die Möglichkeit einen absoluten Mn-Wert zu bestimmen; man bestimmt zunächst den Mw-Wert einer Probe über die statische Lichtstreuung [2], und den Wert für die Polydispersität über eine relative Kalibrierung. Aus diesen beiden Werten kann dann ein absolutes Resultat für den über die statische Lichtstreuung nur schwer zugänglichen Mn-Wert berechnet werden.
Fazit
Mit der Methode der relativen Kalibrierung in der GPC/SEC lassen sich schnell und reproduzierbar Werte für das Molekulargewicht und die Molekulargewichtsverteilung von makromolekularen Proben bestimmen. Das GPC/SEC-System muss nur mit einem einfachen und kostengünstigen Konzentrationsdetektor ausgestattet sein.
Meist wird ein differentieller Brechungsindexdetektor verwendet, seltener ein UV-Detektor. Über die zu vermessende Probe muss der Anwender nur wenig wissen; es reicht, wenn die Probe mit einer für die Erzeugung eines chromatographischen Peaks ausreichenden Konzentration in einem geeigneten Löse- und Laufmittel gelöst wird. Diese muss aber nicht exakt bekannt sein und geht auch nicht in die Berechnung der Molekulargewichte einer Probe ein.
Die Methode der relativen Kalibrierung ist somit eine sehr einfach zu handhabende Methode. Sie hat aber klare Limitierungen. Wie beschrieben werden mit dieser Methode nur dann korrekte, also real vorliegende Molekulargewichte gemessen, wenn Probe und verwendete Standards sowohl chemisch wie auch strukturell gesehen absolut identisch sind. Kurz gesagt kann man nur für lineare Polystyrolproben korrekte Ergebnisse erhalten, wenn man als Kalibrationsstandards lineare Polystyrole verwendet hat.
Sobald sich die Proben entweder chemisch und/oder strukturell von den Kalibrationsstandards unterscheiden, dann erhält man im Prinzip falsche Resultate, die dann aber in Äquivalenten zu den Kalibrationsstandards angegeben werden, und somit zumindest reproduzierbar, wenn auch nicht real oder absolut sind.
Eine weitere, sehr wichtige Einschränkung der Methode der relativen Kalibrierung, ist die Tatsache, dass mit dieser Technik keinerlei Informationen über die chemische Zusammensetzung der Probe und über deren Struktur zugänglich sind. Hat man zwei Proben, deren Elutionsvolumina sich unterscheiden, kann man nicht sagen, ob die Ursache dafür in unterschiedlichen Molekulargewichten, unterschiedlichen chemischen Zusammensetzungen, oder unterschiedlichen Molekülstrukturen zu finden ist.
Jeder dieser Parameter würde zu einer Verschiebung des Elutionsvolumens führen. Daher muss sehr sorgfältig darauf geachtet, werden dass die Ergebnisse der relativen Kalibrierung nicht falsch interpretiert werden.
Literatur
- W. W. Yau, J. J. Kirkland und D. D. Bly "Modern SizeExclusion Liquid Chromatography", John Wiley & Sons, 2009, ISBN: 9780471201724
- P. Kratochvil, "Classical Light Scattering from Polymer Solutions" Elsevier, Amsterdam 1987, ISBN: 9780444428905
